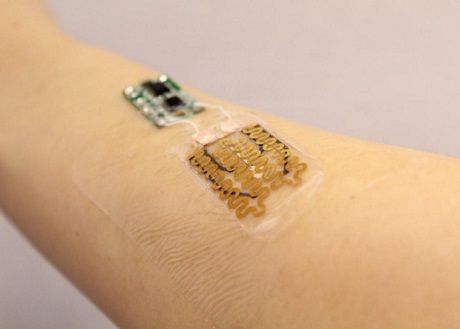
Пластырь состоит их двух основных слоев. В непосредственном контакте с раной находится слой гидрогеля, в котором равномерно распределены сферические полимерные частицы с антибиотиком цефазолином.
Американские инженеры создали активный пластырь для хронических ран, высвобождающий лекарство в случае необходимости. Для отслеживания состояния раны пластырь оснащен датчиками температуры и pH, а также микроконтроллером для обработки данных, рассказывают разработчики в журнале Small.
Человеческая кожа обладает сильной способностью к заживлению умеренных повреждений, но она может быть снижена в случае сильных повреждений, таких как обширные ожоги, также заживлению ран могут мешать различные заболевания — например, диабет. При диабете в тканях ухудшается циркуляция крови, что замедляет заживление ран и снижает локальный иммунитет. Оба этих фактора повышают вероятность развития инфекции в месте ранения.
Группа американских инженеров под руководством Али Хадемхосейни (Ali Khademhosseini) из Калифорнийского университета в Лос-Анджелесе разработала электронный пластырь, который создает барьер для патогенов из окружающей среды и снабжает область раны антибиотиками при необходимости. Инженеры выбрали в качестве маркера инфицирования раны величину pH в ней. При нормальном заживлении pH должен находиться в пределах от 5,5 до 6,5, но в случае инфицированной незаживающей раны он будет выше.
Пластырь состоит их двух основных слоев. В непосредственном контакте с раной находится слой гидрогеля, в котором равномерно распределены сферические полимерные частицы с антибиотиком цефазолином. Для того, чтобы антибиотик не высвобождался самопроизвольно, исследователи выбрали полимер, который переходит из гидрофильного в гидрофобное состояние при изменении температуры. Поскольку критическая температура этого перехода составляет 32 градуса Цельсия, инженеры модифицировали состав другими мономерами и довели эту температуру до 37 градусов.
Разработчики добавили к слою гидрогеля с частицами-носителями антибиотика слой электроники, управляющий высвобождением лекарства. На гибкой полимерной подложке расположены датчики pH и температуры, а также нагреватель. При достижении критического pH нагреватель увеличивает температуру гидрогеля и заставляет капсулы высвобождать антибиотик, который затем попадает на поверхность раны. Датчик температуры при этом используется для отслеживания нагревания. Данные с датчиков считываются и обрабатываются с помощью небольшого модуля с микроконтроллерами, который соединяется с электродами пластыря и закрепляется на коже рядом с ним.
Инженеры провели несколько лабораторных тестов, в том числе подтвердили способность пластыря отслеживать изменения pH, вызванные присутствием золотистого стафилококка. Кроме того, испытания на человеческих клетках-кератиноцитах показали, что пластырь не токсичен по отношению к этим клеткам.
В прошлом году в США провели клинические испытания пластыря с микроиглами, содержащими антигены вирусов. После наклеивания иглы безболезненно проникают в кожу и вводят препарат. Кроме того, существуют несколько прототипов электронных пластырей для измерения уровня глюкозы в крови и даже ввода сахароснижающего препарата, а также для измерения скорости тока крови.